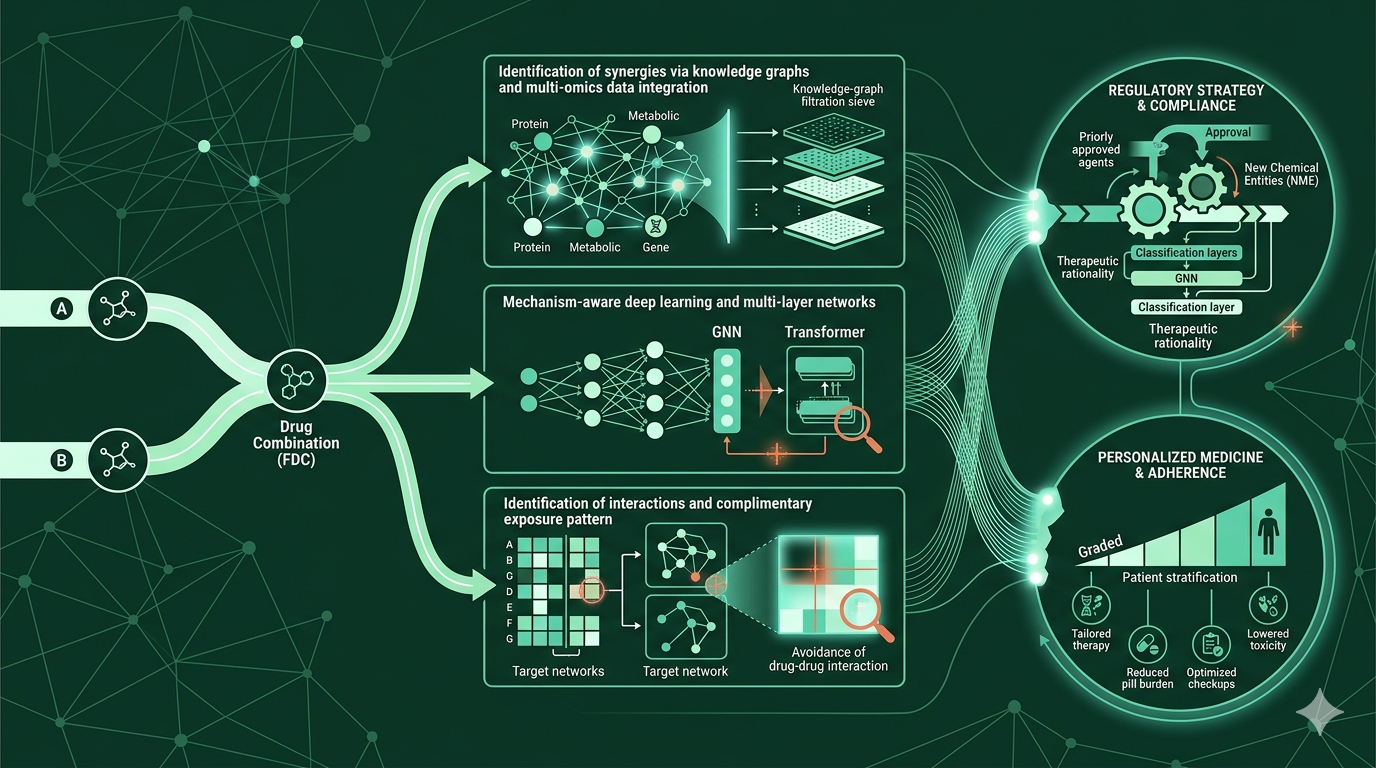
Kombinace léků (drug combinations, fixed-dose combinations – FDC) nabízejí zásadní výhody oproti monoterapiím, zvláště u komplexních, multifaktoriálních chorob, kde souběžná regulace více biologických drah zvyšuje šanci na léčebný úspěch. Synergické kombinace umožňují snížit dávky jednotlivých aktivních látek, což vede nejen ke zvýšení účinnosti, ale také k menšímu riziku toxicity, nižším nákladům a často ke zjednodušení režimu pro pacienty. Fixní kombinace navíc zlepšují adherenci díky nižší lékové zátěži („pill burden“), což potvrzuje řada studií napříč chronickými chorobami.
Vývoj kombinovaných léků je však výrazně komplexnější než tradiční vývoj monoterapií. Rizikem jsou například vzájemné nežádoucí lékové interakce (DDI), chemické neslučitelnosti složek, nebo rozdíly v jejich farmakokinetice a stabilitě. Klíčovou výzvou je i extrémně velké množství potenciálních kombinací, což brání efektivnímu experimentálnímu testování.
V posledních letech proto narůstá význam počítačového modelování, zejména aplikací strojového učení a síťových (network-based) přístupů. Machine learning využívá rozsáhlých databází in vitro synergie a fenotypových dat k predikci synergistických/antagonistických kombinací, přičemž aktuální metodika (od regresních po hluboké modely) stále čelí problémům s obecností, kvalitou dat či interpretovatelností. Významnou roli hrají síťové modely, které mapují interakce mezi lékovými cíli, proteiny, drahami a nemocemi. Tyto modely přináší lepší mechanistické porozumění fungování kombinací – například ukázaly, že nejúčinnější kombinace mají cíle zapojené do stejné patologické sítě, ale bez vzájemného překryvu (tzv. complementary exposure pattern).
Limitací síťových modelů je neúplnost dat o proteinových interakcích či směrovosti vztahů, proto dochází k rozšíření o další vrstvy (knowledge graphs), které zapojují metabolity, biochemické funkce či ontologii onemocnění, a k propojení s omics daty v reálném kontextu. Tyto multivrstvé sítě pomáhají nejen generovat hypotézy, ale i identifikovat rizika DDI a potenciální nežádoucí účinky, s možností lepe rozlišit biologické příčiny interakcí.
Regulatorní schvalování FDC závisí na statusu jednotlivých složek i zamýšlené indikaci. Pokud FDC obsahuje pouze schválené aktivní látky, je možné využít zkrácené procedury, kde lze použít již existující klinická data k podpoře účinnosti, bezpečnosti i bioekvivalence. Pokud se jedná o nové chemické entity (NME), je vyžadována kompletní sada preklinických a klinických studií nejen pro kombinaci, ale často i pro jednotlivé složky. V každém případě musí být terapeutická racionalita kombinace jednoznačně doložena včetně přínosu kombinace oproti monoterapiím.
Historická analýza schvalování kombinačních léčiv FDA od roku 1943 do 09/2024 ukazuje kontinuální nárůst počtu nově povolených kombinací (aktuálně cca 7–10 za rok, což je přibližně 9% nových povolení ročně). Většina FDC vychází z dříve schválených účinných látek, a většina kombinuje léčiva se stejnou nebo podobnou terapeutickou oblastí. Paleta indikací pro FDC se však v posledních dekádách výrazně rozšiřuje, nově zejména do oblasti onkologie, imunologie, kardiologie, diabetologie a antivirotik.
Autoři uzavírají, že kombinované léky se stávají stále důležitějším pilířem moderní farmakoterapie. Síťové modely umožňují mechanisticky zdůvodnit vývoj a schválení kombinací, což je zásadní pro úspěšné povolení a bezpečné nasazení. Budoucí rozvoj vyžaduje lepší harmonizaci regulatorních postupů a další propojení síťových, omických a AI přístupů, což zjednoduší vývoj, zrychlí translaci do klinické praxe a napomůže dostupnosti efektivní kombinované léčby pro široký okruh pacientů.
Zdroje:
Fillinger, L., Walter, S., Ley, M., Keska-Izworska, K., Ghasemi Dehkordi, L., Kratochwill, K., Perco, P. Computational modeling approaches and regulatory pathways for drug combinations. Drug Discovery Today, 2025, 30(5):104345. https://doi.org/10.1016/j.drudis.2025.104345