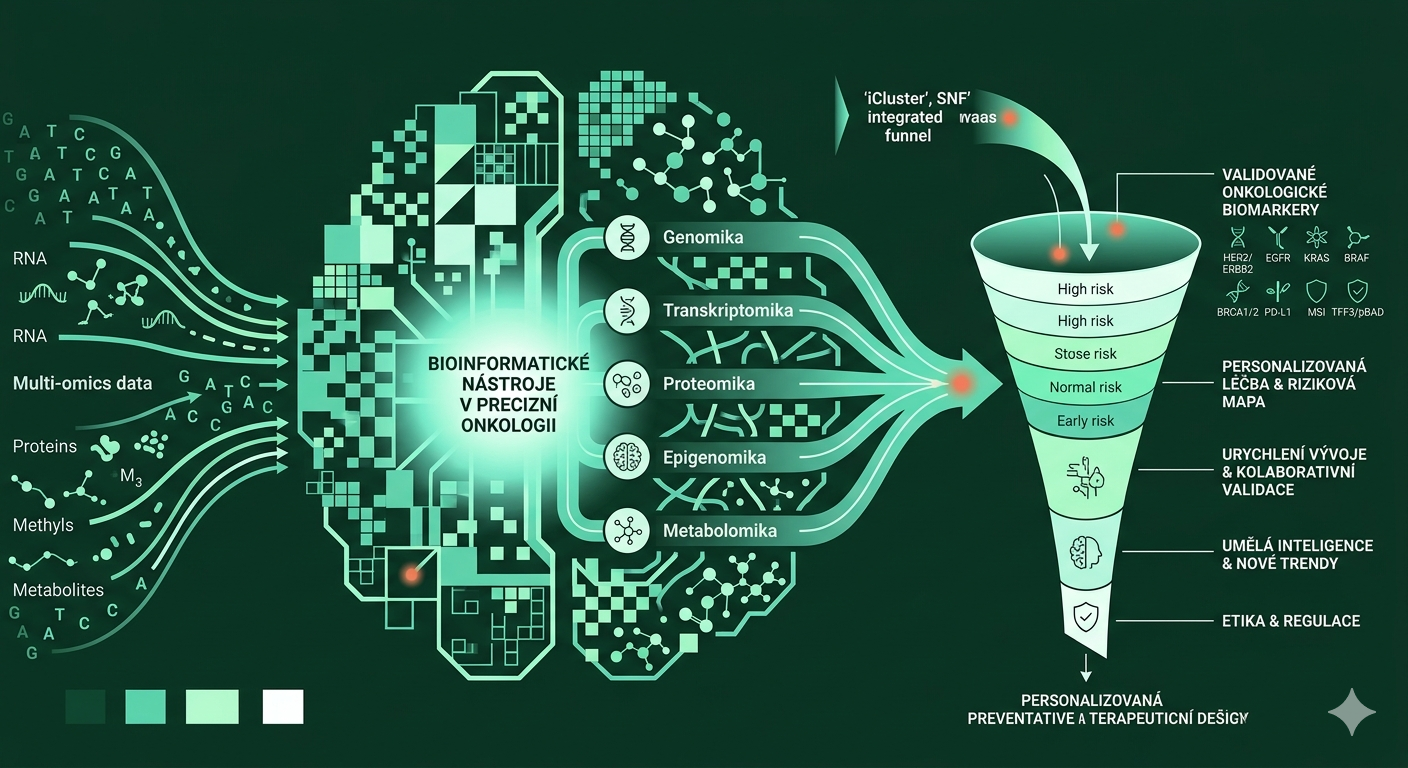
Článek shrnuje zásadní úlohu bioinformatických technik a nástrojů v celém procesu vývoje nových léčiv, včetně urychlení identifikace cílů, screening kandidátů, predikci účinnosti i bezpečnosti, analýzu mechanismů rezistence, a opětovné využití stávajících léčiv. Velký důraz je kladen na integraci omických dat (genomika, transkriptomika, proteomika, metabolomika) a moderních výpočetních metod (molekulární dokování, virtuální screening, masivní databáze), jež umožňují efektivní rozvoj personalizované a přesné medicíny.
Základní bioinformatické komponenty ve výzkumu léčiv
- Biologické databáze: Uchovávají a sdílejí genomová, proteinová, transkriptomická i biomarkerová data. Příklady: GenBank, UniProt, ArrayExpress, KEGG, ChEMBL, HMDB, BioCyc, SuperNatural, NPACT, TCMSP, CancerHSP, PharmacoDB aj. Tyto databáze zásadně podporují vyhledávání potenciálních cílů, modelování vazeb (QSAR, farmakofory), screening a predikci biologických účinků sloučenin.
- Výpočetní nástroje (molekulární dokování a virtuální screening): Pokročilé metody computer-aided drug design (CADD) umožňují rychle a levně modelovat interakce mezi malými molekulami a proteinovými cíli. Docking je základní strukturálně založená metoda pro predikci afinity a vazby (tzv. pose scoring). Podporuje fragment-based screening, optimalizaci základní struktury a stanovuje hypotézy pro další in vitro/in vivo testování, včetně interpretace krystalografických dat. Limitací je zejména přesnost skórovacích funkcí a obtížná predikce u malých fragmentů.
- Omické technologie: Výrazně akcelerují pochopení nemocí i vývoj léčiv:
- Genomika: Identifikuje genové mutace, klíčové cíle v patogenezi, umožňuje srovnávací analýzy mezi patogeny a hostitelem i repurposing léčiv na základě znalosti genové homologní skupiny.
- Transkriptomika: Analyzuje kompletní RNA profil buněk za konkrétních podmínek; odhaluje odlišně exprimované geny (DEGs), nové cíle, využívá se v fenotypovém screeningu i predikci účinku.
- Proteomika: Významná pro ověřování funkce cílových proteinů, predikci jejich 3D struktury a hledání nových molekul pro modulaci jejich aktivity. Téměř všechny malé molekuly či bioaktivní látky cílí na proteiny.
- Metabolomika: Zaměřuje se na odhalení abnormálních metabolitů a biochemických drah; využívá zejména hmotnostní spektrometrii a umožňuje přesnější záchyt změn než genomika/transkriptomika, což je významné pro biomarkery i cíle léčby (včetně neinvazivního monitoringu).
Klíčové aplikace bioinformatiky ve vývoji léčiv
- Vývoj protinádorových léčiv: Integrace multiomics (např. kombinace mRNA, proteomických a fosfoproteomických dat ve studiu malobuněčného karcinomu plic) umožňuje stratifikaci nádorových podtypů a predikci odpovědi na cílenou léčbu (např. inhibitory ATR/TOP1, inhibitory DLL3, RTK, AURKA). Bioinformatika urychluje objev nových cílů i validaci biomarkerů, napomáhá v personalizované léčbě napříč onkologickými diagnózami (prsa, žaludek, plíce, hematologie aj.).
- Infekční a epidemická onemocnění: Analýza genomu patogenů (např. SARS-CoV-2) pro pochopení šíření, evoluce i rezistence; bioinformatika umožnila rekordně rychlou identifikaci cílových struktur viru (sekvenování, predikce proteinové struktury, vývoj vakcín). Dále asistovala u repurposingu léčiv na COVID-19 i v identifikaci sdílených patogenetických mechanismů s jinými nemocemi (např. SLE).
- Rychlý repurposing léčiv: Kombinace omických dat a PPI sítí pomáhá efektivně využít existující léčiva v nových indikacích, což zkracuje vývojový čas a snižuje náklady.
Hlavní výhody a limitace
Výhody:
- Urychlení identifikace lékových cílů, komplexní screening, optimalizace kandidátů, predikce účinnosti a bezpečnosti (včetně nežádoucích účinků a rezistence).
- Jasná opora v personalizované medicíně díky integraci individuálních omických dat.
- Významné zkrácení času a snížení nákladů oproti tradičním přístupům.
Limitace:
- Výzvy v přesnosti skórovacích funkcí při dokování; problém malých fragmentů a rozlišení správných ligandových pozic.
- Vysoké nároky na kvalitu dat, komplexnost a správnou interpretaci multiomics informací.
- Správná identifikace funkčních cílů za přijatelné náklady a využití AI zůstávají otevřenou výzvou.
Závěr
Bioinformatika umožňuje efektivní skladování, správu a analýzu biologických dat, zásadně podporuje všechny fáze objevování a vývoje léčiv od molekulárního screeningu po personalizované strategie léčby v onkologii i infekčních chorobách. Rapidní vývoj technologií posouvá hranice poznání, akceleruje translaci do klinické praxe, avšak klade důraz na přesnost identifikace cílů a efektivní využití AI nástrojů.
Zdroje:
Zhang S, Liu K, Liu Y, Hu X, Gu X. The role and application of bioinformatics techniques and tools in drug discovery. Frontiers in Pharmacology. 2025; 16:1547131. https://doi.org/10.3389/fphar.2025.1547131